Cátedra de Elementos de Química Orgánica y Biológica.
Anuncio

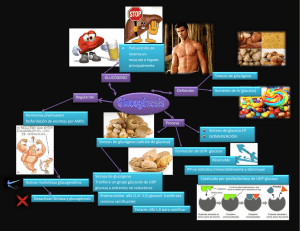
Cátedra de Elementos de Química Orgánica y Biológica. METABOLISMO DE LOS GLÚCIDOS. INTRODUCCIÓN La característica más saliente de los glúcidos es su gran movilidad y su disponibilidad como fuente de energía. A lo largo de este tema se abordan las rutas biosintéticas de los glúcidos. Estas vías permiten el almacenamiento de energía en forma de glucógeno y la reposición de las cantidades de glucosa necesaria para el organismo. La disponibilidad de glucosa es primordial para que las células puedan desarrollar de forma eficaz su metabolismo y sus funciones. Este proceso se lleva a cabo, en parte, regulando la síntesis y degradación del glucógeno, o bien mediante la síntesis de glucosa a partir de precursores hidrocarbonados más simples en una ruta denominada gluconeogénesis. El mantenimiento de una concentración adecuada de glucosa es crucial para el organismo, y la concentración de glucosa disuelta en plasma está sujeta a una regulación precisa. En condiciones normales la concentración es de 80 mg/100 ml (4,5 mM). En una situación de hipoglucemia cuando cae a la mitad de su valor, aparecen molestias y aturdimiento; si sigue disminuyendo se entra en una situación de coma y convulsiones pudiendo llegar a la muerte. El metabolismo del glucógeno, la gluconeogénesis y las rutas degradativas estudiadas, están perfectamente coordinadas y reguladas, según las necesidades energéticas o sintéticas que tengan las células en cada momento. Así en la sangre la glucosa está siempre presente y en cualquier momento puede ser utilizada por las células; además éstas pueden almacenarla, en mayor o menor grado, en forma de glucógeno. Algunos tejidos especializados en la realización de una gran cantidad de trabajo, como el músculo o las glándulas, poseen un contenido relativamente alto de glucógeno. Antes de que los glúcidos simples o monosacáridos puedan ser utilizados por la célula para obtener energía o bien para la síntesis de glucógeno, se tienen que transformar previamente en derivados fosforilados. La glucosa en presencia de la enzima glucoquinasa y ATP se transforma en glucosa-6-fosfato. La galactosa se convierte en galactosa-1-fosfato, que se transforma en glucosa-1-fosfato y ésta a su vez en glucosa-6-fosfato. Todas las células animales pueden almacenar glucógeno que se sintetiza a partir de glucosa a través de la siguiente vía metabólica: glucosa ATP y glucosa-6-fosfato, glucosa-6-fosfato y glucosa-1-fosfato; glucosa-1-P UTP y UDP-glucosa; UDP-glucosa y glucógeno. Cuando se presenta la necesidad de glucosa, el glucógeno, en una reacción catalizada por la enzima 1 Cátedra de Elementos de Química Orgánica y Biológica. fosforilasa, se transforma en glucosa-1-fosfato y ésta en glucosa-6-fosfato. La conversión de esta última en glucosa sólo puede realizarse en el hígado. La glucosa-6 fosfato puede seguir la vía degradativa que se conoce con el nombre de glicolisis, en la que a través de una serie de pasos catalizados por enzimas específicas, una molécula de seis átomos de carbono se convierte en dos moléculas de tres carbonos. Si estas reacciones tienen lugar en ausencia de oxígeno el producto final es el ácido láctico. En condiciones anaerobias el piruvato se transforma en ácido láctico en una reacción catalizada por la enzima láctica deshidrogenasa y en la que interviene la coenzima NADH, que a su vez se oxida para dar NAD. La presencia de oxígeno determina la entrada del pirúvico en la vía oxidativa final hasta convertirse en C02 y agua, a través de una serie de reacciones que se conocen con el nombre de ciclo del ácido tricarboxílico, ciclo del ácido cítrico o ciclo de Krebs en honor a su descubridor. El siguiente paso más allá de la glicolisis consiste en la conversión del ácido pirúvico en acetilcoenzima A (acetil-CoA) en una reacción en la que se desprende CO2 y la coenzima NAD se reduce a NADH. El acetil-CoA se condensa con el oxaloacetato para dar citrato En esta secuencia cíclica de reacciones se desprenden dos moléculas C02 en cada vuelta, al mismo tiempo que se reducen tres moléculas de NAD a NADH y una de FAD a FADH2, y se regenera el oxaloacetato que reacciona con una nueva molécula de acetil-CoA para dar comienzo a una nueva vuelta del ciclo. Un sistema de transportadores, que se conoce con el nombre de cadena transportadora de electrones, localizado en las mitocondrias de la célula, se encarga de reoxidar los coenzimas reducidos (NADH, FADH2) transfiriendo electrones de éstos hasta el oxígeno, formándose agua como consecuencia. Este paso de electrones está perfectamente acoplado de modo que simultáneamente se produce la síntesis Biosíntesis de Glúcidos A) En las plantas: Podemos decir que la fotosíntesis es el proceso que mantiene la vida en nuestro planeta. Las plantas terrestres, las algas de aguas dulces, marinas o las que habitan en los océanos realizan este proceso de transformación de la materia inorgánica en materia orgánica y al mismo tiempo convierten la energía solar en energía química. Todos los organismos heterótrofos dependen de estas conversiones energéticas y de materia para su subsistencia. Los organismos 2 Cátedra de Elementos de Química Orgánica y Biológica. fotosintéticos liberan oxígeno al ambiente, del cual también depende la mayoría de los seres vivos de este planeta. Este tema se verá con detalles en la materia Fisiología Vegetal. B) En animales: B.1. A través de la GLUCONEOGÉNESIS: Es una reacción anabólica. Es la vía que permite la síntesis de glucosa a partir de precursores no glucídicos en animales. Muchos tejidos animales no necesitan glucosa, mientras que otros son completamente glucosa dependiente (cerebro, eritrocitos, médula renal). Las reservas glucídicas hepáticas (190 gramos) se agotan en un plazo temporal muy corto, aproximadamente un día, y en periodos más largos sin ingesta de glúcidos, debe formarse glucosa a partir de compuestos no glucídicos para mantener la glucemia. Las células hepáticas disponen, además del metabolismo del glucógeno, de otros mecanismos metabólicos que les permiten disponer de glucosa. La ruta anabólica encargada de esta función es la gluconeogénesis (formación nueva de glucosa), por la cual la glucosa se sintetiza a partir de compuestos no glucídicos, tales como aminoácidos, lactato, piruvato o glicerol. Se desarrolla en un 90% en el hígado y en un 10 % en el riñón. Esta ruta gluconeogénica es crucial para la supervivencia, ya que permite pasar la noche y otros espacios temporales entre las ingestas, manteniendo un nivel mínimo de glucemia (en condiciones de ayuno sostenido a través de la gluconeogénesis se forman unos 50 gramos/día) para el funcionamiento de cerebro, médula renal, testículos y eritrocitos. El agotamiento de las reservas glucídicas no sólo se produce por falta de entrada de alimentos, también puede originarse por consumo incrementado como en periodos de ejercicio intenso, en esta situación es igualmente importante elpapel jugado por la gluconeogénesis. Se puede sintetizar glucosa a partir de: -Lactato. -Piruvato. -Algunos aminoácidos. -Intermedios del ciclo de Krebs. -Glicerol. La gluconeogénesis ocurre sólo en algunos órganos muy concretos, sobretodo en hígado. La corteza renal también puede llevarla cabo. 3 Cátedra de Elementos de Química Orgánica y Biológica. 4 Cátedra de Elementos de Química Orgánica y Biológica. La glucólisis es una ruta universal en los seres vivos, que convierte la glucosa en piruvato y la gluconeogénesis es también una ruta universal, sólo que al revés convirtiendo el piruvato en glucosa; aunque comparten muchas reacciones estas rutas antagónicas no son iguales, y no pueden considerarse procesos inversos. A nivel de la glucólisis hay tres pasos que son prácticamente irreversibles, y que, por lo tanto, requieren estrategias distintas para realizarlos en la gluconeogénesis. Las reacciones que convierten la glucosa en glucosa-6-fosfato, la fructosa-6-fosfato en fructosa 1,6, bisfosfato y, en último lugar, el fosfoenolpiruvato en piruvato. Estos tres pasos en la gluconeogénesis utilizan enzimas diferentes a las glucolíticas, con equilibrios distintos y también son irreversibles, pero en la dirección gluconeogénica o de síntesis de glucosa. El proceso de gluconeogénesis, con la excepción del paso de transfomación de piruvato a oxalacetato (OAA), que ocurre en la membrana mitocondrial, ocurre en el citosol. Una vez que se produce fosfoenolpiruvato (PEP), hay una serie de reacciones seguidas en equilibrio, hasta llegar a la Fructosa-1,6-bisfosfato. Para transformar este compuesto en Fructosa-6-Fosfato, hay un gasto de 1 ATP . La segunda reacción que se realiza con gasto de energía es la transformación de glucosa-6fosfato a glucosa. Esta reacción está catalizada por Glucosa-6-fosfato fosfatasa, que está ubicada en el retículo endoplasmático y no está presente en todos los órganos. Ni músculo ni cerebro pueden liberar glucosa a partir de Glucosa-6-fosfato. 1º Paso: Fosforilación del piruvato a fosfoenolpiruvato: La reacción glucolítica inversa se caracterizaba por la gran variación negativa de energía libre, que la convertía en un proceso irreversible. Para solventar este primer paso se requiere una secuencia de reacciones en la que participan enzimas mitocondriales y citoplasmáticos: a) El piruvato situado en el citoplasma entra en la mitocondria a través del transportador correspondiente, a continuación la piruvato carboxilasa convierte el piruvato en oxalacetato: Piruvato + HCO3 + ATP → Oxalacetato + ADP + Pi + H+ b) El oxalacetato se reduce a malato, mediante la malato deshidrogenasa mitocondrial que utiliza como coenzima NADH, una de las reacciones (reversibles) del ciclo del ácido cítrico: Oxalacetato + NADH + H+ Malato + NAD+ 5 Cátedra de Elementos de Química Orgánica y Biológica. c) El malato sale de la mitocondria utilizando el transportador malato-α-cetoglutarato y en el citoplasma, se reoxida a oxalacetato mediante la enzima malato deshidrogenasa citoplasmática: Malato + NAD+ Oxalacetato + NADH + H+ d) Por acción de la fosfoenolpiruvato carboxiquinasa, el oxalacetato se convierte en fosfoenolpiruvato con consumo de energía: Oxalacetato + GTP Fosfoenolpiruvato + CO2 + GDP La ecuación global para el conjunto de las reacciones descritas sería: Piruvato + ATP + GTP + HCO3 → Fosfoenolpiruvato + ADP + GDP + Pi + H+ + CO2 El ciclo de carboxilar y después descarboxilar constituye un sistema de activar a la molécula con gasto de energía. Mientras que la conversión de fosfoenolpiruvato en piruvato en la glucólisis rendía 1 ATP, en la reacción inversa de la gluconeogénesis se produce el consumo de dos enlaces de alta energía. Ahora, si el precursor gluconeogénico es lactato, su oxidación a piruvato en el citoplasma (reacción inversa a la de la fermentación láctica), proporciona NADH y la secuencia queda resumida como sigue: Lactato → Piruvato → Piruvato mitocondrial → Oxalacetato → Fosfoenolpiruvato mitocondrial → Fosfoenolpiruvato citoplasmático. 2º Paso: Hidrólisis de la fructosa-1,6-bisfosfato a fructosa-6-fosfato. Esta reacción es catalizada por la fructosa-1,6-bifosfatasa, Fructosa-1,6-bisfosfato + H2O ------- Fructosa-6fosfato + Pi 3º Paso: Desfosforilación de la glucosa-6-fosfato a glucosa libre. Esta reacción catalizada por la glucosa-6-fosfatasa es realizada en el retículo endoplasmático de los hepatocitos, y es la misma que se ha descrito en la glucogenolisis a nivel hepático, justificando que el hígado pueda liberar a la corriente sanguínea glucosa libre, procedente de sus reservas glucogénicas o procedente de la ruta gluconeogénica. Para que la glucosa pase a la sangre no debe estar fosforilada: 2 Pir + 4 ATP + 2 GTP + 2 NADH + 6 H2O --> GLUCOSA + 4 ADP + 2 GDP + 6 Pi +2 NAD+ + 2 H+ El glicerol que usan las células para formar glucosa proviene de los triglicéridos. No todos los aminoácidos se convierte en glucosa: la Leucina y la Lisina son aminoácidos cetogénicos. Los aminoácidos glucogénicos dan todos sus Carbonos para la glucosa. El lactato formado por los músculos activos (glucolisis anaeróbica) puede reciclarse, se transporta al hígado en donde se 6 Cátedra de Elementos de Química Orgánica y Biológica. convierte en glucosa (mediante el proceso de gluconeogénesisi) durante la recuperación después de la actividad muscular. Esta glucosa va a sangre y se puede volver a usar por el músculo para obtener energía mediante la glucólisis. Este proceso se denomina ciclo del lactato o ciclo de Cori. 7 Cátedra de Elementos de Química Orgánica y Biológica. -En animales Omnívoros: sólo se realiza la gluconeogénesis cuando no hay aporte de glucosa por la dieta. Esta se realiza a partir del glicerol y/o aminoácidos. – En los Rumiantes: los microorganismos del rumen transforman la glucosa en lactato y acetato, propionato y butirato. Por ello, la gluconeogénesis siempre debe ser muy activa, para poder obtener nuevamente glucosa. Además, en lactantes, se produce mucha lactosa con el consiguiente gasto de glucosa -Los animales Carnívoros: Deben fabricar glucosa a partir de glicerol o aminoácidos (proteínas de la dieta). Regulación de la gluconeogénesis El desarrollo al mismo tiempo de glucólisis y gluconeogénesis supone un gasto energético que no tiene lugar en la célula hepática en condiciones normales. La regulación de ambas rutas se realiza de manera coordinada y recíproca, garantizándose que el funcionamiento de una bloquee la otra, de igual forma que en la síntesis y degradación del glucógeno. Para ello los metabolitos que favorecen o estimulan las enzimas glucolíticos, actúan inhibiendo las enzimas de la gluconeogénesis y viceversa. Los efectores más importantes son los energéticos, aunque también hay un estrecho control hormonal (ver diapositivas). METABOLISMO DEL GLUCÓGENO El glucógeno es un polisacárido de moléculas de glucosa. Es el sistema de reserva de carbohidratos de las células animales (glucosa). Las plantas lo acumulan en forma de almidón. El glucógeno es el polisacárido de reserva animal pudiendo llegar a ser el 10% de la masa del hígado o el 1% de la masa muscular. Es una macromolécula ramificada y compacta que puede llegar a tener hasta 6 x 105 restos de glucosa. Almacenando la glucosa en forma de polímero de alto peso molecular, se pueden condensar multitud de unidades de hexosa sin cambiar la osmolaridad de la célula, ya que ésta no depende del tamaño de las moléculas sino de su número; por otra parte, la liberación de los monómeros constituyentes de la molécula es muy rápida, ya que resulta fácilmente movilizable. Los gránulos de glucógeno están almacenados en el citoplasma de las células hepáticas y musculares, unidos a las enzimas responsables de la síntesis y degradación. 8 Cátedra de Elementos de Química Orgánica y Biológica. Es un sistema de reserva de movilización rápida. En pocos minutos, pasa de estar acumulado a circular. Después de periodos de aproximadamente 12 h, las reservas de glucógeno prácticamente están agotadas. Está presenta prácticamente en todos los tejidos, pero sobretodo en hígado y músculo esquelético. El sentido metabólico del glucógeno hepático es muy diferente al del músculo esquelético. Hay más concentración en hígado que en músculo esquelético. La movilización del glucógeno implica que las glucosas que se liberan son Glucosa1-P. En el hígado donde existe Glucosa6-P fosfatasa, la glucosa-1-P se puede transformar en glucosa y pueden pasar directamente al torrente circulatorio. El músculo lo tiene que consumir directamente en la miofibrilla donde se almacena ya que carece de Glucosa 6 fosfatasa. El glucógeno hepático sirve para abastecer a todo el cuerpo. La degradación del glucógeno está catalizada por la glucógeno fosforilasa según: Glucógeno (n) + Pi Glucosa1P + glucógeno (n-1) La enzima cataliza la rotura del enlace glucosídico α (1 4) del extremo no reductor (OH del carbono 4) de la molécula de glucógeno, separando una molécula de glucosa-1-fosfato y dejando la cadena de glucógeno más corta, con una unidad menos de glucosa.La fosforilasa no hidroliza el glucógeno, sino que lo fosforila. La molécula es atacada por Pi que rompe el enlace y da lugar a una molécula de Glucosa1P. El residuo de glucosa ya sale fosforilado con un costo energético = 0. (Recordar que por lo general fosforilar glucosa requiere un gasto energético, ATP). La enzima se caracteriza porque cataliza una reacción muy cercana al equilibrio. Por eso, durante mucho tiempo se pensó que la glucosa fosforilasa podía no solo degradar sino también formar glucógeno. Sólo puede fosforilar enlaces α 1=>4 pero, por motivos estéricos, la glucosa fosforilasa, cuando llega una molécula de glucosa que está a 4 residuos a contar desde el punto de fosforilación, no puede fosforilarla. Existe otra proteína que ayuda a la glucosa fosforilasa a solucionar su problema (enzima de ramificante). Es una transferasa que recoge las moléculas indigeribles por la glucosa fosforilasa. 9 Cátedra de Elementos de Química Orgánica y Biológica. Glucogenolisis Glucógeno (n) Glucógeno fosforilasa Pi El enlace 1 4 que une dos residuos de glucosa es atacado por el fosfato inorgánico eliminando el residuo de glucosa terminal en forma de -D-glu 1fosfato Glucosa-1-fosfato + Glucógeno (n-1) fosfoglucomutasa La fosfoglucomutasa requiere como cofactor glucosa 1,6-bifosfato. Su actividad es regulada por fosforilaciondesfosforilación de un residuo de Serina Glucosa 6 fosfato Glucosa 6 fosfatasa (hígado, riñón, intestino) Glucosa El residuo que queda de la ramificación es hidrolizada por una actividad α (1=>6) glucosidasa y da lugar a la formación de glucosa. La actividad transferasa y la actividad α (1=>6) glucosidasa, están presentes en la enzima desramificante. La gran mayoría de residuos del glucógeno son liberados como glucosa-1-P. Otro gran porcentaje son liberados como glucosa. Por lo tanto acá tenemos otra fuente de glucosa. Síntesis de glucógeno o glucogénesis En los animales el excedente de glucosa se almacena en forma de glucógeno, siendo especialmente relevante en el hígado y en el músculo esquelético. En el hígado, sirve como almacén de glucosa para todo el organismo, mientras que en el músculo funciona como depósito propio para desarrollar la contracción muscular. La ruta biosintética es una ruta muy diferente de la degradativa. Para realizar la polimerización 10 Cátedra de Elementos de Química Orgánica y Biológica. de la glucosa se necesita la participación del ribonucleótido UTP (uridín trifosfato) que activa las moléculas de glucosa permitiendo la formación de glucógeno. A continuación, la glucógeno sintasa cataliza la formación de un enlace glucosídico α(1--4) en una cadena en crecimiento, y en esta reacción de elongación se desprende el nucleótido UDP. La glucógenosintasa sólo puede añadir unidades de glucosa sobre una cadena mínima de glucógeno formadapor cuatro restos de glucosa que funcionan como un cebador. La síntesis “de novo” desde la primera unidad de glucosa, la realiza la glucogenina, una proteína que cataliza la unión de ocho unidades de glucosa, siendo abastecida de igual forma por moléculas de UDP-glucosa ; la glucógeno sintasa que se encuentra unida a la glucogenina formando un complejo proteico, comienza entonces su actividad catalítica, de elongación de la molécula. La glucogenina permanece unida a la molécula de glucógeno en crecimiento. La formación de ramas la realiza un enzima ramificante que cataliza la creación de enlaces α(1→ 6). La acción de la enzima ramificante exige que la cadena α(1→ 4), o cadena lineal en crecimiento, tenga al menos once residuos para poder realizar el corte de los siete últimos y formar un enlace α(1→ 6). El costo energético de almacenar la glucosa en forma de glucógeno es relativamente bajo, ya que la incorporación de cada unidad de glucosa al polímero, es de un enlace de alta energía (el consumido del UTP a UDP). En la oxidación total de la molécula de glucosa se generan unas 36 moléculas de ATP, si el almacenamiento supone el gasto de 1, la eficacia total es del 97%. Regulación del metabolismo del glucógeno 11 Cátedra de Elementos de Química Orgánica y Biológica. Las dos principales enzimas que controlan la biosíntesis y la degradación del glucógeno son la glucógeno sintasa y la glucógeno fosforilasa. Ambas son enzimas alostéricas que están reguladas por la acción de un par de enzimas quinasa/fosfatasa que incorporan o eliminan, respectivamente, un grupo fosfato sobre determinados residuos aminoacídicos. En ambas enzimas los procesos son antagónicos, así para la glucógeno sintasa su forma activa es la forma desfosforilada o glucógeno sintasa a, y la forma inactiva es la fosforilada o glucógeno sintasa b. Para la glucógeno fosforilasa es exactamente al contrario, fosforilada es activa, o forma a, y desfosforilada es la inactiva, o forma b. De esta manera no se encuentran ambas activadas al mismo tiempo. Dra. Roxana Mabel Ordóñez Prof. Adjunta Cátedra de Elementos de Qca. Orgánica y Biológica 12