NEUROPATÍAS ÓPTICAS POR TRASTORNOS FÍSICOS
Anuncio

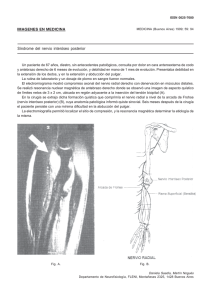
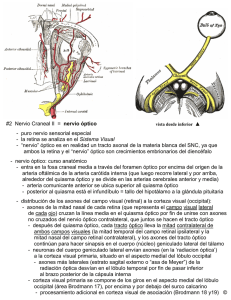
CAPÍTULO 13 NEUROPATÍAS ÓPTICAS POR TRASTORNOS FÍSICOS NEUROPATÍA ÓPTICA TRAUMÁTICA Miguel Esteban, Manuel Cervera, Víctor Menezo AFECTACIÓN DEL NERVIO ÓPTICO POR OTROS AGENTES Jorge Arruga, Nuria Ibáñez En el presente capítulo se estudiarán las afecciones del nervio óptico que reconocen como factores etiopatogénicos a los agentes físicos. Entre éstos destacan por su importancia las lesiones producidas por traumatismos craneoencefálicos (TCE) accidentales, frente a las consecutivas a otros agentes cuya incidencia es menos frecuente. NEUROPATÍA ÓPTICA TRAUMÁTICA El interés del estudio de los traumatismos del nervio óptico radica en las graves secuelas visuales que producen y en que afectan sobre todo a un sector de la población joven y laboralmente activo. Sin embargo, debido a su baja incidencia, no resulta fácil establecer un protocolo terapéutico que permita mejorar el pronóstico visual de los pacientes con este tipo de neuropatía. Clasificación de los Traumatismos del Nervio Óptico Se pueden establecer diferentes clasificaciones, una primera según el tipo de traumatismo, una segunda según su localización y una tercera, que combina las otras dos. De acuerdo con el tipo de traumatismo, se distinguen dos variedades, los directos y los indirectos. Los traumatismos directos son debidos a heridas accidentales órbito-faciales penetrantes que lesionan directamente la integridad anátomo-funcional del nervio óptico (1). En cambio, los indirectos son habitualmente TCE cerrados, cuyo mecanismo implica, sobre todo, desaceleración craneal, y la lesión es consecutiva a la trasmisión de las fuerzas del impacto traumático a distancia hasta el nervio óptico. De acuerdo con la localización de la lesión, es preciso hacer referencia a los 4 segmentos en los que se divide el trayecto del nervio óptico, o sea, el intraocular, el intraorbitario, el intracanalicular y el intracraneal (ver capítulo 2). Las características anatómicas diferenciales de estos segmentos determinan la afectación de cada uno de ellos según el tipo de traumatismo producido (2). Así, a nivel del segmento intraorbitario, la forma sinusoidal condicionada por su longitud excesiva comparada con la distancia entre el globo ocular y el agujero óptico, confiere al nervio una relativa protección en los traumatismos indirectos. En el segmento intracanalicular, el periostio del canal óptico está firmemente adherido a la duramadre del nervio y esta fijación e inmovilidad hacen al mismo muy vulnerable a las fuerzas traumáticas indirectas trasmitidas. Finalmente, el segmento intracraneal del nervio presenta también una mayor vulnerabilidad ante estos traumatismos, debido a su proximidad respecto al pliegue falciforme de la duramadre que cubre la apófisis clinoides anterior. Frente a un enfoque simplista de la cuestión, la clasificación mixta nos proporciona un mejor conocimiento de las lesiones producidas en el nervio óptico. Así, por ejemplo, un TCE cerrado (indirecto) lleva a veces asociada una fractura esfenoidal que lesiona el nervio óptico (directo). Los traumatismos indirectos, además de afectar al nervio en su porción intracanalicular, pueden producir en determinadas situaciones un arrancamiento de la porción intraocular. Ninguna clasificación nos permite saber cuál es el mecanismo defi- 282 Neuropatías ópticas: diagnóstico y tratamiento Figura 13-1. Mecanismos de lesión reversible del nervio óptico. (A) Compresión por edema. (B) Compresión por hemorragia. (C) Compresión por desplazamiento óseo. [Modificada de Parra Duque LA. En: Stamm AC, Draf W (eds.). Micro-endoscopic surgery of the paranasal sinuses and skull base. Berlin: Springer, 2000: p. 441-9]. nitivo de la lesión celular y cuáles son en última instancia las posibilidades de recuperación funcional del nervio óptico. A pesar de todo ello, utilizaremos la clasificación siguiente, que combina el tipo de traumatismo producido con la localización de la lesión en el nervio óptico, a saber: • Traumatismos directos del nervio óptico • Traumatismos indirectos anteriores del nervio óptico • Traumatismos indirectos posteriores del nervio óptico Patogenia y Mecanismos de Lesión Celular Las fuerzas desacelerativas aplicadas al hueso frontal son trasmitidas y concentradas en el hueso esfenoides a nivel de la región del canal óptico. En esta región la cubierta meníngea del nervio óptico está íntimamente unida al canal óseo, lo que condiciona la posibilidad de una necrosis contusional inmediata del nervio. Las lesiones traumáticas de este último tienen un doble modo de producción, mecánico e isquémico, aunque según la relación temporal con el traumatismo, los mecanismos se dividen en primarios y secundarios (fig. 13-1). Los mecanismos primarios son inmediatos con respecto al impacto traumático. Se produce una lesión axonal directa, así como lesiones hemorrágicas e isquémicas, todo lo cual acarrea una necrosis irreversible de un número determinado de axones del nervio óptico. No existen posibilidades de tratamiento frente a estas lesiones primarias. Los mecanismos secundarios se producen en una etapa más tardía respecto del traumatismo. Consisten en fenómenos de vasospasmo y edema del nervio óptico, con el consiguiente síndrome compartimental, dado que el canal óptico es una estructura inextensible. La isquemia resultante desencadena la liberación de radicales libres de oxígeno, que a su vez provocan la peroxidación de los lípidos de la membrana celular axonal, y se produce asimismo un aumento de la concentración intracelular de los iones de calcio. Todo ello aboca a la muerte secundaria de los axones que habían sobrevivido a las lesiones primarias. Las diferentes modalidades terapéuticas (corticoterapia a altas dosis, descompresión quirúrgica) actúan en esta fase impidiendo que estos axones no dañados de forma primaria lo sean de forma secundaria (1-4). Existen otros mecanismos poco frecuentes capaces de producir una afectación tardía del nervio óptico, como son las fístulas carótido-cavernosas y los aneurismas postraumáticos (5). Traumatismos Directos La trayectoria de una herida abierta a nivel facial, orbitario o cerebral afecta al recorrido del nervio óptico, como primera posibilidad, a través de un mecanismo inmediato consistente en la penetración del objeto externo, por ejemplo una bala, y la lesión directa de los axones del nervio. Como segunda posibilidad, la afectación se produce por mecanismos consecutivos, que incluyen entre otros, la impactación en el nervio de las espículas procedentes de una fractura ósea y los hematomas orbitarios postraumáticos. Una variedad excepcional de lesión traumática directa la constituye el arrancamiento posterior del nervio óptico (fig. 13-2). El concepto tradicional de las lesiones del nervio óptico asociadas a TCE está siendo sustituido por las cada vez más frecuentes descripciones bibliográficas de complicaciones yatrógenas. Éstas tienen lugar en el curso de Capítulo 13. Neuropatías ópticas por trastornos físicos 283 Traumatismos Indirectos Posteriores Figura 13-2. Arrancamiento del nervio óptico y de los músculos oculares extrínsecos como consecuencia de la impactación de un cuerpo extraño de madera en la órbita. procedimientos quirúrgicos en la vecindad del nervio, que por lesión directa o indirecta conducen a una pérdida visual irreversible. Son ejemplos de tales procedimientos la cirugía endoscópica de los senos paranasales, la reparación de las fracturas orbitarias, la utilización de la radiofrecuencia para la neuralgia del trigémino o la clásica lesión del nervio óptico en la anestesia retrobulbar para la cirugía del globo ocular (6-8) (ver también capítulo 10). La aparición de una dilatación pupilar ipsilateral al finalizar un acto quirúrgico de vecindad debe hacer sospechar la existencia de una lesión en el nervio óptico. No obstante, hay que diferenciar esta midriasis de la causada por los fármacos adrenérgicos, cuya utilización es habitual en la cirugía endoscópica sinusal (9). En las diferentes variedades de traumatismos directos la pérdida visual es total la mayor parte de las veces. Traumatismos Indirectos Anteriores Las lesiones situadas en la porción anterior del nervio óptico, por delante de la penetración de la ACR en el mismo (10 mm detrás del globo ocular) tienen unas características especiales en cuanto a su mecanismo de producción y a su manifestación oftalmoscópica (10,11). La avulsión del nervio óptico es consecutiva a rotaciones extremas o a desplazamientos violentos anteriores del globo ocular, casi siempre debidos a objetos romos causantes de un arrancamiento del nervio a nivel de la lámina cribosa. Estas lesiones producen una pérdida visual inmediata y severa asociada a lesiones en el fondo ocular. Las lesiones del nervio óptico situadas por detrás de la entrada de la ACR se caracterizan por aparecer tras TCE cerrados con un mecanismo brusco de desaceleración y por no causar apenas cambios inmediatos en el fondo del ojo. Desde el punto de vista clínico se presentan como una pérdida de visión inmediata al traumatismo con o sin evidencia de afectación ocular u orbitaria que la justifique. Se trata de una verdadera neuropatía retrobulbar y asocia los signos clásicos, tales como discromatopsia, alteraciones campimétricas inespecíficas y DPAR. La incidencia de los traumatismos indirectos posteriores es la más alta entre todas las variedades de lesiones traumáticas del nervio óptico, los cuales se localizan por lo general a nivel de su porción intracanalicular (1-3,12). Epidemiología Debido al escaso número de casos descritos en la literatura, se desconocen en la actualidad la incidencia y la prevalencia reales de la neuropatía óptica traumática (NOT) en la población, aunque se aprecia una mayor incidencia en los individuos del sexo masculino (85%), por debajo de los 35 años. Se estima que dicha neuropatía aparece en el 2-5% de los TCE cerrados, aunque su incidencia aumenta hasta el 20% en series que incluyen fracturas maxilofaciales y frontobasales complejas (13). El tipo de TCE inicial está siempre relacionado con un mecanismo brusco de desaceleración (v. gr.: accidente de tráfico, caída, etc.), por impacto ipsilateral a nivel fronto-facial. Éste puede ser leve, aunque habitualmente es grave, ya que se trata de pacientes politraumatizados con pérdida de la conciencia en hasta el 50% de los casos. La disminución de la visión es severa e inmediata, excepción hecha de unos pocos casos con pérdida visual diferida (10%), y el 70% de las veces la agudeza inicial es inferior a movimientos de mano (14). Diagnóstico Clínico El diagnóstico de la NOT se sospecha cuando una pérdida de la visión coincide con un TCE y no existe evidencia de afectación óculo-orbitaria que pueda ser 284 Neuropatías ópticas: diagnóstico y tratamiento Figura 13-3. Avulsión total del nervio óptico. Oquedad en la pared del globo ocular, a nivel de la zona correspondiente a la papila, con hemorragia intraocular masiva, tras un traumatismo orbitario con un palo de hockey. su causa. Siempre habrá que descartar otras posibilidades, como una lesión más posterior de las vías ópticas o una pérdida visual no orgánica. Existen casos leves sin disminución de la agudeza visual, pero que presentan otros signos clínicos de NOT (discromatopsia, DPAR, etc.). Los problemas diagnósticos surgen al tratarse muchas veces de enfermos politraumatizados con pérdida de la conciencia y que precisan de otros cuidados prioritarios cardiovasculares o respiratorios de interés vital. Es importante determinar, con la ayuda de algún familiar del paciente, si éste tenía defectos visuales previos, así como el tipo de TCE que padeció, sobre todo por razones médicolegales (1,2). Figura 13-4. Traumatismo indirecto de la parte anterior del nervio óptico, de naturaleza contusa, que revela una palidez del disco óptico, con edema habitualmente de grado moderado. La agudeza visual de estos enfermos debe de ser tomada en cuanto sus condiciones generales lo permitan, aunque el diagnóstico de neuropatía óptica unilateral requiere la existencia de un DPAR ipsilateral al nervio cuya lesión se sospecha. Por otro lado, la presencia de un DPAR en un enfermo comatoso tras un TCE, cuya agudeza visual no se puede determinar, es un signo inequívoco de lesión a nivel del nervio óptico ipsilateral, en ausencia de otras alteraciones oftalmoscópicas. Cuando la pupila no reacciona en absoluto al estímulo directo, pero sí lo hace al consensual, estamos ante la certeza de que el paciente tiene una pérdida visual severa y no percibe la luz. En casos menos graves, un método sencillo muy útil para detectar la presencia de una neuropatía óptica es la realización de pruebas de visión cromática, que se afectan de forma precoz y son de una gran sensibilidad. Cuando sea posible se debe practicar una campimetría, pues, si bien no hay ninguna alteración patognomónica de traumatismo del nervio óptico (pueden aparecer defectos altitudinales, centrales, paracentrales, centrocecales y hemianópsicos), permite controlar la evolución del proceso. Por descontado, hay que efectuar siempre una exploración oftalmológica completa que descarte cualquier otra causa intraocular de pérdida visual postraumática. Por lo que se refiere al fondo ocular, la avulsión parcial del nervio óptico (15,16) se manifiesta como un anillo hemorrágico que ocupa un sector de la papila, mientras que la avulsión total (fig. 13-3) produce una hemorragia papilar completa. Ésta última, al reabsorberse, deja ver una depresión oscura a nivel del disco óptico y, conforme van cicatrizando los tejidos, el área papilar queda cubierta por un tejido glial que proviene de los márgenes retinianos. Otras formas de presentación de los traumatismos anteriores del nervio (fig. 13-4) incluyen la oclusión de la ACR y la NOIA (17). Cuando existe un hematoma dentro de la vaina meníngea perióptica se puede observar desde un edema papilar hasta una oclusión de la VCR (1). En cambio, los traumatismos posteriores del nervio (fig. 13-5) se caracterizan inicialmente por un aspecto normal de la papila, hasta que trascurridas 3 a 5 semanas a partir del accidente aparece la atrofia óptica. Los PEV pueden ser útiles para el diagnóstico de NOT en un paciente inconsciente, especialmente si la lesión es bilateral, ya que entonces la ausencia de DPAR hace más difícil dicho diagnóstico. Sin embargo la realización de esta prueba está limitada en muchas Capítulo 13. Figura 13-5. Traumatismo indirecto de la parte posterior del nervio óptico tras una contusión craneal, sin alteraciones neurorradiológicas. El OD afecto de amaurosis (A) muestra una dilatación de las venas retinianas, comparado con el OI (B). El disco óptico derecho evolucionó hacia la atrofia sin recuperación visual. Neuropatías ópticas por trastornos físicos 285 Figura 13-6. Esquirla procedente de una fractura ósea, impactada en el nervio óptico izquierdo cerca de su entrada en el canal óptico. (Reproducida de López et al. (18)). ocasiones por razones logísticas, ya que el mal estado general de estos enfermos hace que no sea posible su traslado fuera de la unidad de cuidados intensivos. La ausencia de respuesta eléctrica en los PEV constituye un signo inequívoco de pérdida completa de visión, con un pronóstico muy desfavorable en cuanto a su recuperación. En cambio, si se obtiene una respuesta eléctrica es posible utilizarla también para valorar la progresión de la función del nervio (1). Diagnóstico Radiológico (18) La realización de una TC es imprescindible en la evaluación de todo paciente afecto de un TCE, ya que nos permite el estudio de la órbita y las estructuras adyacentes si existe sospecha de NOT. La mejora de la visualización del canal óptico que ha posibilitado la TC ha revelado que las fracturas a nivel del canal (fig. 13-6) son mucho más frecuentes de lo que se pensaba con la radiología simple. La fractura en algunos casos lesiona directamente el nervio óptico, mientras que en otros constituye un reflejo de la intensidad de la fuerza traumática absorbida por el segmento intracanalicular del nervio. La TC es claramente superior a la RM en la evaluación de fracturas óseas y proporciona información sobre otros posibles mecanismos de afectación del nervio óptico (figs. 13-7 y 13-8). No obstante, la RM nos permite una mejor interpretación de las Figura 13-7. Hematoma postraumático del músculo recto externo, que provoca una protrusión del globo ocular derecho, con angulación de la esclerótica, de casi 90º, y elongación del nervio óptico. (Reproducida de López et al. (18)). Figura 13-8. Colección hemática a nivel de la inserción en el globo ocular del nervio óptico izquierdo y avulsión de este último, consecutivas a un traumatismo cráneofacial. (Caso de los Dres. E. López y E. España. Valencia). 286 Neuropatías ópticas: diagnóstico y tratamiento alteraciones en los tejidos blandos adyacentes (v. gr.: hemorragia en la vaina del nervio óptico). Antes de realizar esta última exploración, hay que descartar siempre la presencia de un cuerpo extraño metálico (2). Tratamiento El tratamiento de la NOT indirecta es motivo de controversia y la utilización de una u otra alternativa terapéutica está basada en las publicaciones sobre pequeñas series retrospectivas o sobre casos clínicos aislados. La falta de estudios prospectivos y el desconocimiento de los mecanismos últimos de lesión intracelular hacen complicados el análisis y la interpretación comparativos de los resultados obtenidos mediante la terapéutica médica, la quirúrgica o la simple observación sin tratamiento. Los resultados de un análisis retrospectivo sugerían que los casos sometidos a tratamiento médico, quirúrgico o combinado tenían una evolución más favorable que los no tratados (19). Con el fin de dilucidar cuál de los enfoques terapéuticos es el más apropiado se creó el International Optic Nerve Trauma Study (20), que en un principio pretendió llevar a cabo un estudio randomizado y controlado. Sin embargo, después de 2 años de reclutar pacientes se abandonó el proyecto, dado que el escaso número de casos y las dificultades para su randomización lo hacían estadísticamente inviable, incluso a largo plazo, por lo que quedó finalmente convertido en un estudio de observación. Sus conclusiones fueron que los pacientes con una neuropatía óptica traumática indirecta, tanto si no son tratados, como si reciben corticosteroides o si se someten a una descompresión quirúrgica del canal óptico difieren poco en cuanto a su agudeza visual final. Más aún, la ecuación riesgo-beneficio se decantaría hacia la simple observación, ya que de este modo se evitan las posibles complicaciones inherentes al uso de corticoides sistémicos o a la cirugía. Existe, por otro lado, experiencia sobre casos de NOT con buena respuesta inicial a los corticoides, pero con deterioro tardío de la visión (21). La utilización de altas dosis de corticoides sistémicos (ver capítulo 15) está muy extendida desde que se demostró que la utilización de metilprednisolona (MPDN) en megadosis durante las 8 horas siguientes a un traumatismo de la médula espinal (estudio NAS- CIS 2) mejoraba su evolución. Sin embargo existen diferencias fundamentales entre dos estructuras como la médula espinal y el nervio óptico, por lo que los resultados no son superponibles. Hasta que se realice un estudio randomizado a doble ciego sobre la utilización de los corticoides a altas dosis en la NOT debemos considerar este tratamiento como empírico (3,22,23). A su vez, la cirugía por descompresión del canal óptico (DCO) (ver capítulo 16) se basa en la mejoría que debe experimentar el nervio óptico traumatizado y edematoso al practicar una abertura en el canal, un compartimiento cuya inextensibilidad condiciona el daño axonal secundario. Para el acceso hasta la pared del canal se han utilizado la vía intracraneal y diversas vías extracraneales, como la transetmoidal, la transetmoido-esfenoidal o la transnasal endoscópica. La indicación de cualquiera de estas intervenciones es también empírica, pues no existen estudios que demuestren de forma definitiva cuándo ni cómo se deben de realizar (24-28). A falta de estudios prospectivos adecuados, las graves secuelas que produce este tipo de traumatismos motivan que en la mayoría de los centros médicos se utilicen protocolos de tratamiento, variantes del de Steinsapir, que combinan ambas modalidades terapéuticas (1,29), como el siguiente: • De cara al tratamiento es fundamental la detección precoz de la lesión, en pacientes por lo general politraumatizados e inconscientes. • Lo más importante es indicar la cirugía ante toda patología «tratable», es decir, aquellas lesiones identificadas mediante los estudios de neuroimagen, que pueden producir daño secundario al nervio óptico. Así, es preciso practicar cantotomías laterales para las hemorragias orbitarias, fenestraciones de la vaina en las hemorragias de la misma (ver capítulo 16), o drenajes de los hematomas subperiósticos. • Se recomienda administrar una megadosis de corticoides intravenosos, comenzando por 1 g de MPDN y pasando luego a 250 mg cada 6 horas, durante 48 h. • Si a las 48 h no hay mejoría de la agudeza visual puede estar indicada una DCO quirúrgica. • Si a las 48 h hay mejoría de la agudeza se pasa a una pauta de prednisona oral, pero en caso de recaída visual se debe reinstaurar la MPDN y plantear la cirugía, consistente en extirpación de las esquirlas óseas que impactan el nervio y descompresión del canal óptico. Capítulo 13. AFECTACIÓN DEL NERVIO ÓPTICO POR OTROS AGENTES Dentro de este grupo de procesos estudiaremos en primer lugar los que sobrevienen a consecuencia del tratamiento con radioterapia o de las quemaduras térmicas accidentales. En segundo lugar, abordaremos aquéllos que acontecen como complicación del desprendimiento posterior del vítreo, y los que se presentan tras la cirugía filtrante o refractiva, en relación con una disminución o con un aumento de la PIO, respectivamente. Otras neuropatías ópticas que se producen como complicación de procedimientos quirúrgicos se comentan en el capítulo 10 y en el apartado de neuropatía óptica traumática. Neuropatía Óptica por Irradiación Es una afección poco frecuente del nervio óptico que se produce como complicación diferida del tratamiento radioterápico efectuado sobre el cerebro o sobre la órbita. La mayor parte de las veces tiene lugar después de la irradiación de tumores hipofisarios o de neoplasias nasofaríngeas (30), aunque se observa también en casos de otras lesiones paraselares, de los lóbulos temporales e intraoculares (31). El SNC se puede afectar a consecuencia de la irradiación según tres formas clínicas (32). En primer lugar, los efectos agudos aparecen en el curso de irradiaciones cerebrales completas durante los primeros días y son causados por un edema cerebral reversible. En segundo lugar, los efectos diferidos precoces se producen en los 4 meses siguientes a la radioterapia local, tienen por mecanismo una desmielinización focal y regresan casi siempre, ya sea espontáneamente o con la corticoterapia. En tercer lugar, los efectos diferidos tardíos se constatan tras un intervalo de varios meses a varios años respecto al tratamiento radioterápico, y su patogenia consiste sobre todo en una necrosis irreversible, con un deterioro funcional progresivo y posterior estabilización en algunos casos. La afectación del nervio óptico por la radioterapia tiene lugar por un efecto diferido, casi siempre tardío, con una incidencia máxima entre los meses 8.º y 13 que siguen a dicha modalidad terapéutica (33). El riesgo de esta neuropatía es mayor si se utilizan dosis totales superiores a 50 Gy, o si los fracciona- Neuropatías ópticas por trastornos físicos 287 mientos diarios superan los 1,8 Gy para la radioterapia convencional (34), o bien si la irradiación excede 10 Gy en dosis única para la radiocirugía (35). Las dosis tóxicas son algo menores cuando los nervios ópticos están previamente afectados a causa de la compresión por parte de tumores. Son factores de riesgo adicionales la edad inferior a 12 años, la hipertensión arterial (HTA), la diabetes y la quimioterapia asociada (36). De todos modos, la irradiación sobre los nervios es en ocasiones superior a la prevista debido a errores técnicos, por lo que no se puede descartar la neuropatía óptica aun con dosis comprendidas dentro de los márgenes terapéuticos. La pérdida de la visión suele ser indolora, subaguda y progresiva, con afectación de un ojo o de los dos, y en este último caso se puede producir de modo simultáneo o sucesivo. El cuadro clínico corresponde en los casos tardíos al de una neuropatía óptica isquémica anterior o posterior, de modo que es posible observar un edema isquémico del disco óptico (NOIA) (fig. 13-9), aunque con mayor frecuencia el fondo ocular al inicio es normal (NOIP). Los campos visuales revelan contracciones concéntricas, defectos altitudinales (fig. 13-10) o escotomas centrales y, cuando se afecta el quiasma, hemianopsias bitemporales. La evolución es siempre inexorable hacia la atrofia óptica en 4-6 semanas (30), con una visión final inferior a 0,1 la mayoría de las veces, y una amaurosis en cerca de la mitad. No existe en la literatura acerca de esta enfermedad una sola descripción sobre recuperación espontánea de la función visual (33). La RM en las neuropatías ópticas diferidas tardías por irradiación demuestra alteraciones cuando se utili- Figura 13-9. Papilopatía por irradiación. Edema papilar con hemorragias y microinfartos tras la irradiación de un melanoma maligno de la coroides con un implante episcleral de 125I. 288 Neuropatías ópticas: diagnóstico y tratamiento Figura 13-10. Campimetría a umbral de una neuropatía óptica retrobulbar por irradiación. Defecto hemianópsico altitudinal superior, de probable mecanismo isquémico, en un paciente tratado con radioterapia por un carcinoma de las fosas nasales. (Programa G1. Octopus Field Analyzer). za la secuencia T1 con refuerzo de gadolinio (37) (ver capítulo 4), las cuales son reversibles. De hecho, los estudios histológicos practicados sobre nervios ópticos irradiados han demostrado una disminución de las células endoteliales en los vasos, indicativa de una disrupción a nivel de la barrera hematoencefálica (38). En casos de neuropatía óptica comprobada, la anatomía patológica ha consistido en desmielinización por isquemia, astrocitosis reactiva, hiperplasia endotelial, endarteritis obliterante y necrosis fibrinoide (30). El diagnóstico diferencial de esta neuropatía óptica se ha de efectuar sobre todo con respecto a la recidiva del tumor inicial, a una neoplasia radioinducida y, en casos de lesiones de la región selar, al síndrome de la silla turca vacía secundario o a la aracnoiditis optoquiasmática. La corticoterapia o la anticoagulación han producido, en general, resultados decepcionantes y algunos autores han empleado la oxigenoterapia en cámara hiperbárica, con eficacia controvertida. De acuerdo con la revisión de Borruat, la oxigenoterapia es el único tratamiento que permite obtener en determinados casos una recuperación de la función visual. Para ello, dicho autor recomienda que se administre oxígeno al 100% a una presión mínima de 2,4 atmósferas, lo más precozmente posible, en 30 sesiones de 90 minutos cada una (33). Una variante de pérdida visual con atrofia óptica consecutiva a la radioterapia es la que puede tener lugar por un mecanismo oclusivo a nivel de las arteriolas retinianas tras la irradiación de tumores cervicales (fig. 13-11). En estos casos se produce una angiopatía por irradiación diferida y tardía con implicación de las. arterias carótidas extracraneales, que experimentan una aceleración del proceso habitual de aterosclerosis (32). Neuropatía Óptica por Quemadura Durante la fase aguda de su proceso, los quemados graves pueden experimentar una pérdida visual como consecuencia de edema e hipoxia cerebrales, acompañada de otros signos de encefalopatía. No obstante, se ha descrito también una forma infrecuente y severa de neuropatía óptica bilateral (39), cuya presentación es más diferida, después de quemaduras no necesariamente extensas. Suele cursar con edema papilar y hemorragias retinianas, y en su patogenia, probablemente multifactorial, se ha sugerido que interviene el efecto desmielinizante de una neurotoxina elaborada a nivel de la zona lesionada (40). Papilopatías Secundarias a Alteraciones Mecánicas Intraoculares Figura 13-11. Angiopatía por irradiación. Envainamiento periarteriolar bilateral con defectos altitudinales en los campos visuales tras la radioterapia practicada sobre adenopatías cervicales en una paciente afecta de enfermedad de Hodgkin. El desprendimiento del vítreo, en su parte posterior, puede causar hemorragias yuxtapapilares y edema peripapilar, aunque éste constituye una complicación extremadamente rara, si se tiene en cuenta la elevada Capítulo 13. Figura 13-12. Hipotonía ocular consecutiva a una intervención quirúrgica filtrante por un glaucoma. Edema papilar difícil de enfocar, debido a la presencia de pliegues en la córnea. frecuencia de la patología mencionada (41). Asimismo, la hipotonía ocular severa (fig. 13-12) reconoce como causas las heridas perforantes o contusiones del globo, y en especial las intervenciones filtrantes con un efecto hipotensor ocular excesivo. En estos casos se suele constatar una disminución visual, por la presencia de edema con pliegues corneales, y un edema de la papila atribuible a un bloqueo del flujo axonal a nivel de la lámina cribosa (42). Por último, se ha descrito recientemente una neuropatía óptica aguda, unas veces anterior y otras retrobulbar, que sobreviene en casos excepcionales a continuación de un procedimiento de cirugía refractiva mediante LASIK. No se han identificado factores de riesgo y en su patogenia se ha incriminado a la elevación de la PIO inducida por el anillo de succión. Ello podría producir, por un lado, una compresión de las células ganglionares, las fibras nerviosas y la lámina cribosa, con lesión papilar consiguiente, y por otro lado, una isquemia secundaria a la interrupción del flujo sanguíneo en la ACR y en las ACP (43). Para su prevención se recomienda reducir en lo posible el tiempo de succión y se cuestiona la investigación preoperatoria de factores de riesgo de isquemia en el nervio óptico (HTA, diabetes, dislipemia, relación excavación/disco baja) (44). BIBLIOGRAFÍA 1. Steinsapir K, Goldberg RA. Traumatic optic neuropathies. En: Miller NR, Newman NJ, eds. Walsh and Hoyt’s Clinical Neuro-Ophthalmology. 5th ed. Baltimore: Williams & Wilkins, 1998: p. 715-39. Neuropatías ópticas por trastornos físicos 289 2. March GA, Scott C, Goldberg RA. Traumatic optic neuropathy. Facial Plastic Surgery Clinics of North America 1998; 6: 31-9. 3. Steinsapir K. Traumatic optic neuropathy. Curr Opin Ophthalmol 1999; 10: 340-2. 4. Steinsapir K, Goldberg RA. Traumatic optic neuropathy. Surv Ophthalmol 1994; 38: 487-518. 5. Eidlitz-Markus T, Shuper A. Delayed visual loss after blunt head trauma. Neuroophthalmology 2000; 23: 15-20. 6. Rene C, Rose GE, Lenthall R et al. Major orbital complications of endoscopic sinus surgery. Br J Ophthalmol 2001; 85: 598-603. 7. Egan RA, Pless M, Shults WT. Monocular blindness as a complication of trigeminal radiofrequency rhizotomy. Am J Ophthalmol 2001; 131: 237-40. 8. Liu D. Blindness after blow-out fracture repair. Ophthalmol Plast Reconstr Surg 1994; 10: 206-10. 9. Badia L, Lung VJ. Dilated pupil during endoscopic sinus surgery: what does it mean?. Am J Rhinol 2001; 15: 31-3. 10. Roth DB, Warman R. Optic nerve avulsion from a golf injury. Am J Ophthalmol 1999; 128: 657-8. 11. Friedman SM, Optic nerve avulsion secondary to a basketball injury. Ophthalmic Surg Lasers 1999; 30: 676-7. 12. Hamard H, Chevaleraud J, Rondot P (eds.). La neuropathie traumatique. En: Neuropathies optiques. Paris: Societé Française d’Ophtalmologie / Masson, 1986: p. 395-411. 13. Amrith S, Saw SM, Lim TC et al. Ophthalmic involvement in cranio-facial trauma. J Cranio Maxillo Fac Surg 2000; 28: 140-7. 14. Wang BH, Robertson BC, Girotto JA et al. Traumatic optic neuropathy. Plast Reconstr Surg 2001; 107: 1655-64. 15. Sayagués A, Maiz D, Teigell J et al. Avulsión parcial de la cabeza del nervio óptico. Arch Soc Esp Oftalmol 1992; 63: 541-6. 16. Bueno E, Asensio VM, Green RL et al. Avulsión parcial del nervio óptico. Arch Soc Esp Oftalmol 1995; 69: 539-44. 17. Martínez J, Ascaso F, Carbonell P. Neuropatía óptica isquémica traumática: aplicación de la ecografía Dopplercolor. Oftalmología Práctica 1997; 7: 14-8. 18. López E, España E, Muñoz F et al. Eficacia de la tomografía computerizada (T.A.C.) en el diagnóstico urgente de la neuropatía óptica traumática. Arch Soc Esp Oftalmol 2001; 76: 621-6. 19. Cook MW, Levin LA, Joseph MP et al. Traumatic optic neuropathy. A meta-analysis. Arch Otolaryngol Head Neck Surg 1996; 122: 389-92. 20. Levin LA, Beck R, Joseph M et al. The treatment of traumatic optic neuropathy. Ophthalmology 1999; 106: 1268-77. 21. Mariak, Z, Obuchowska I, Mariak Z et al. High-dose steroid therapy of traumatic optic neuropathy may fail to protect the optic nerve permanently. Neuroophthalmology 1999; 21: 255-60. 22. Seiff SR. Therapy for traumatic optic neuropathy. Arch Ophthalmol 1991; 109: 610. 23. Spoor TC, Hartel WC, Lensink DB et al. Treatment of traumatic optic neuropathy with corticosteroids. Am J Ophthalmol 1991; 111: 526. 290 Neuropatías ópticas: diagnóstico y tratamiento 24. Joseph MP, Lessell S, Rizzo J et al. Extracranial optic nerve decompression for traumatic optic neuropathy. Arch Ophthalmol 1990; 108: 1086-7. 25. Kountakis SE, Maillard AA, El-Harazi SM et al. Endoscopic optic nerve decompression for traumatic blindness. Otolaryngol Head Neck Surg 2000; 123: 34-7. 26. Li KK, Teknos TN, Lai A et al. Extracranial optic nerve decompression. J Craniofac Surg 1999; 10: 454-9. 27. Villarreal PM, De Vicente JC, Junquera LM. Traumatic optic neuropathy. Int J Oral Maxillofac Surg 2000; 29: 29-31. 28. Girard B, Lamas G, Bouzas E et al. Surgical descompression of the optic nerve in intracranial injuries. Indications and results. J Fr Ophtalmol 1992; 15 : 83-92. 29. Mauriello JA, DeLuca J, Krieger A et al. Management of traumatic optic neuropathy. Br J Ophthalmol 1992; 76: 349-52. 30. Kline LB, Kim JY, Ceballos R. Radiation optic neuropathy. Ophthalmology 1985; 92: 1118-26. 31. Lommatzsch PK, Alberti W, Lommatzsch R et al. Radiation effects on the optic nerve observed after brachytherapy of choroidal melanomas with 106Ru/ 106Rh plaques. Graefe’s Arch Clin Exp Ophthalmol 1994; 232: 482-7. 32. Peterson K, Rottenberg DA. Radiation damage to the brain. En: Vecht CJ (ed.). Handbook of Clinical Neurology. Vol. 23. Amsterdam: Elsevier Science, 1997: p. 325-51. 33. Borruat FX, Schatz NJ, Glaser JS et al. Radiation optic neuropathy: report of cases, role of hyperbaric oxygen therapy, and literature review. Neuroophthalmology 1996; 16: 255-66. 34. Parsons JT, Bova FJ, Fitzgerald CR et al. Radiation optic neuropathy after megavoltage external-beam irradiation: 35. 36. 37. 38. 39. 40. 41. 42. 43. 44. Analysis of time-dose factors. Int J Radiation Oncology Biol Phys 1994; 30; 755-63. Leber KA, Berglöff J, Pendl G. Dose-response tolerance of the visual pathways and cranial nerves of the cavernous sinus to stereotactic radiosurgery. J Neurosurg 1998; 88: 43-50. Ebner R, Slamovits TL, Friedland S et al. Visual loss following treatment of sphenoid sinus carcinoma. Surv Ophthalmol 1995; 40: 62-8. Guy J, Mancuso A, Beck R et al. Radiation-induced optic neuropathy: a magnetic resonance imaging study. J Neurosurg 1991; 74: 426-32. Levin LA, Gragoudas ES, Lessell S. Endotelial cell loss in irradiated optic nerves. Ophthalmology 2000; 107: 370-4. Salz JJ, Donin JF. Blindness after burns. Can J Ophthalmol 1972; 7: 243-6. Unsöld AS, Rizzo JF, Lessell S. Optic neuropathy after burns. Arch Ophthalmol 2000; 118; 1696-8. Katz B, Hoyt WF. Intrapapillary and peripapillary hemorrhage in young patients with incomplete posterior vitreous detachment. Signs of vitreopapillary traction. Ophthalmology 1995; 102: 349-54. Minckler DS, Bunt AH. Axoplasmic transport in ocular hypotony and papilledema in the monkey. Arch Ophthalmol 1977; 95: 1430-6. Cameron BD, Saffra NA, Strominger NB. Laser in situ keratomileusis-induced optic neuropathy. Ophthalmology 2001; 108: 660-5. Lee AG, Kohnen T, Ebner R et al. Optic neuropathy associated with laser in situ keratomileusis. J Cataract Refract Surg 2000; 26: 1581-4.