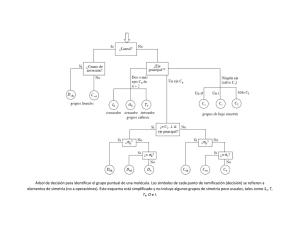
Simetría Molecular b a c d
Anuncio

Cátedra de Química Inorgánica II – Material Complementario - Simetría Molecular Simetría Molecular Como material anexo para la resolución de los problemas del Seminario #1: “Simetría Molecular”, y el Trabajo Práctico #1 “Análisis de los espectros IR del metano y productos de sustitución” presentamos el siguiente material complementario. Las ilustraciones son capturas de pantalla del software libre molWAVE® (disponible en la web http://www.molwave.com/), se recomienda visitar el sitio para ver las animaciones de las diferentes operaciones de simetría y de los modos vibracionales de algunas moléculas de interés. Moléculas con plano de simetría (σ = S1) → no presentan isomería óptica 1,3,5,7-Cicloocatetraeno - C8H8 Pertenece al grupo de simetría D2d y sus elementos son E, S4, C2 y σd. La molécula no es ópticamente activa y la presentamos por ser similar al 1,3,5,7-Tetrametilcicloocta-cis,cis,cis,cis-1,3,5,7-tetraeno, que tampoco es quiral (verificar). a b c d En las figuras a) y d) se observan los tres ejes C2 perpendiculares desde dos ángulos distintos, y en la figura b) una vista superior de uno de los ejes. En la figura c) se pueden ver los dos planos de simetría de la molécula. Cátedra de Química Inorgánica II – Material Complementario - Simetría Molecular Ejemplo de molécula sin plano de simetría (σ = S1) ni centro de inversión (i = S2), pero con eje de rotación impropio Sn → no presenta isomería óptica. Efecto del cambio de una posición de enlace. Tetrafenilmetano - C(C6H5)4 Pertenece al grupo de simetría S4 y los elementos presentes son E, C2 y S4. La molécula no presenta plano de simetría ni centro de inversión, pero como tiene un eje impropio de rotación no es quiral. a b c d En las figuras a) y b) se muestran las operaciones sucesivas de rotación y reflexión en el plano resaltado, que componen la operación S4 característica del grupo al que pertenece la molécula. Trifenilmetano - CH(C6H5)3 En las figuras c) y d) de la figura anterior, se presenta la molécula resultante de sustituir un grupo fenilo por un H, trifenilmetano y pertenece al grupo C3, su simetría es menor que la del Tetrafenilmetano. Además del elemento identidad E sólo cuenta con un eje de rotación C3, sin ejes de rotación impropios, por lo tanto es quiral. Cátedra de Química Inorgánica II – Material Complementario - Simetría Molecular Modos vibracionales del metano y uno de sus derivados por sustitución de un H por otro átomo. Análisis de geometrías para Metano y Clorometano - CH4 y CH3Cl Pertenecen a los grupos de simetría Td y C3v respectivamente. El primero tiene los elementos E, C3, C2, S4 y σd, mientras que el segundo es menos simétrico y sólo tiene los elementos E, C3 y σv. En la siguiente figura se muestran las dos moléculas con algunos elementos señalados. Cátedra de Química Inorgánica II – Material Complementario - Simetría Molecular Modos vibracionales del Metano El metano presenta 3N-6 grados de libertad, de los cuáles 3 son rotacionales, 3 son translacionales y los restantes 9 son vibracionales. Utilizando la tabla de caracteres para las representaciones irreducibles del grupo de simetría Td, construyendo una representación reducible para la molécula y aplicando las reglas derivadas del Gran Teorema de la Ortogonalidad para las operaciones entre representaciones de un grupo, se puede deducir la siguiente relación: Γvib = A1 + E + 2T2. Activo en RAMAN Activo en RAMAN Activo IR y en RAMAN Puede predecirse la presencia de cuatro señales en RAMAN y dos en IR. Ahora, pueden deducirse las geometrías aproximadas de estos modos vibracionales verificando la transformación de las coordenadas internas según las operaciones de simetría del grupo. Las coordenadas internas serían las cuatro distancias C—H y los seis ángulos H—C—H (notar que en este caso no todos los ángulos pueden variar independientemente, por lo tanto aparecerán modos sin sentido físico en el análisis que deberán ser descartados). Operando con las representaciones reducibles se pueden obtener las siguientes representaciones reducibles: Metano, Td ΓC-H ΓH-C-H E 4 6 ΓH-C-H 8C3 1 0 3C2 0 2 6S4 0 0 6σd 2 2 ΓC-H = A1 + T2 = A1 + E + T2 = E + T2 (eliminando A1). La representación totalmente simétrica A1 no puede ser parte de los modos de deformación H—C—H porque no pueden variar todos los ángulos de igual forma al mismo tiempo, por eso se elimina de la expresión para ΓH-C-H. Por lo anterior, los modos vibracionales de deformación pueden expresarse utilizando las representaciones irreducibles E y T2, mientras que los de estiramiento con las representaciones irreducibles A1 y T2. Los estiramientos tienen mayor k (constante de fuerza) que las deformaciones, por eso aparecen a frecuencias mayores en el espectro vibracional (ν = c (k / µ) 0.5). En las siguientes figuras se muestran capturas de pantalla donde aparecen los modos normales de vibración para la molécula de metano (A1, E doblemente degenerado y T2 triplemente degenerado), con flechas se encuentran resaltados las direcciones de cada átomo en el movimiento (se recomienda ingresar a la web de molWAVE para ver las animaciones). Cátedra de Química Inorgánica II – Material Complementario - Simetría Molecular T2, deformaciones triplemente degeneradas (una señal a ≈1300 cm-1) RAMAN e IR E, deformaciones doblemente degeneradas (≈1530 cm-1) RAMAN solamente Cátedra de Química Inorgánica II – Material Complementario - Simetría Molecular zz A1, estiramiento simétrico, sólo RAMAN (≈2900 cm-1) T2, estiramientos triplemente degeneradas (≈3020 cm-1) RAMAN e IR