Teórica 14 regulacion local flujo.pdf
Anuncio
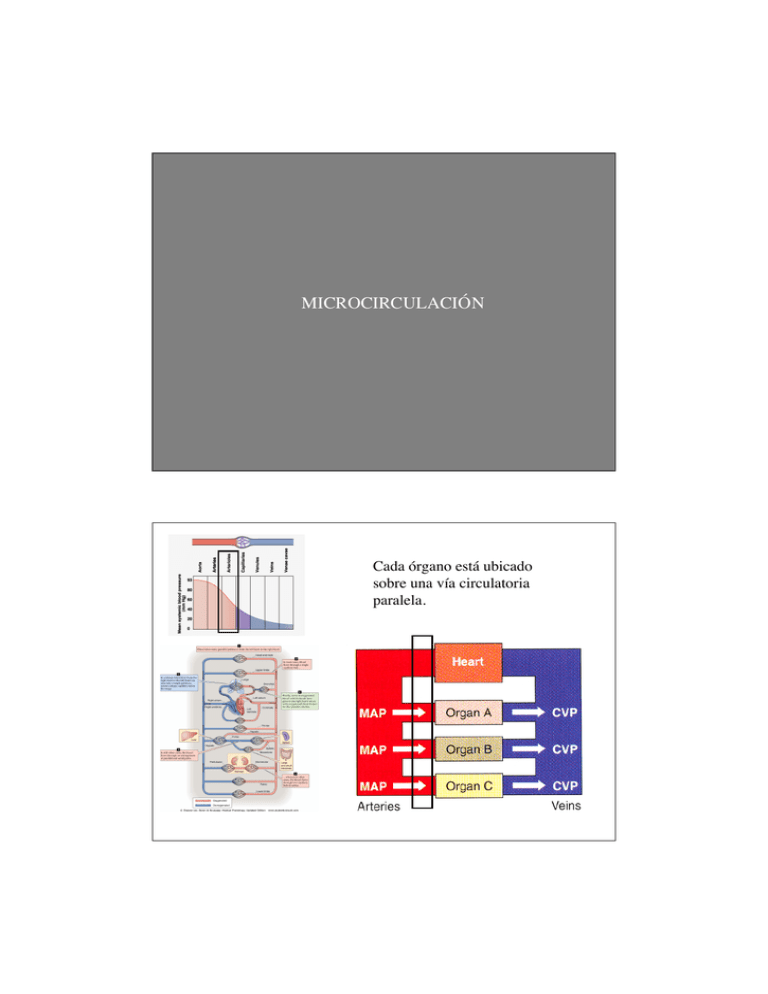
MICROCIRCULACIÓN Cada órgano está ubicado sobre una vía circulatoria paralela. Distribución del gasto cardíaco en reposo y ejercicio físico corazón derecho corazón izquierdo pulmón reposo 5% cerebro 8% corazón RETORNO VENOSO ejercicio 5% sistema digestivo 2% sistema excretor musculatura 80% piel 25 l /min GASTO CARDIACO: R1 Q = ΔP / R R2 Q = QA + QB QA = ΔP / RA QB = ΔP / RB Flujo = ΔP / R R= 8Lη πr4 resistencia periférica total REGULACION DEL FLUJO SISTEMICO DIFERENCIAL • Regulación local • Regulación neural • Regulación hormonal y por sustancias vasoactivas REGULACION DEL FLUJO SISTEMICO DIFERENCIAL aorta arteriola control de la resistencia capilar vénula vena v. cava vasodilatación vs vasoconstricción REGULACION DEL FLUJO SISTEMICO DIFERENCIAL aorta arteriola capilar Reclutamiento de capilares vénula vena Controlado por la presión arterial local v. cava Variaciones en la resistencia de las arteriolas modifica la presión en capilares. Vasodilatación de la arteriola I Vasoconstricción de la arteriola I CONTROL LOCAL DE LA RESISTENCIA DE LAS ARTERIOLAS BIOMECANICOS • Reflejo miogénico • Shear stress HUMORALES METABOLICOS REGULACION DEL FLUJO SISTEMICO DIFERENCIAL La regulación de la resistencia se controla mayoritariamente a nivel de las arteriolas interacciones celulares en la pared vascular endotelio músculo liso espacio intersticial lumen Figueroa, X. F. et al. Physiology 19: 277-284 2004 CONTROL LOCAL DEL FLUJO lumen endotelio músculo liso el control de la resistencia se efectúa por contracción y relajación del músculo liso vascular Control biomecánico Las paredes de los vasos están sujetas a dos fuerzas presión hidrostática lumen vascular shear stress endotelio músculo liso Reflejo miogénico Respuesta del músculo liso al estiramiento de la pared vascular. presión hidrostática lumen vascular endotelio músculo liso Diámetro del vaso (µm) Reflejo miogénico pasivo bajo [Ca++] control sin endotelio Cambio de presión hidrostática sin flujo Reflejo miogénico Diámetro del vaso (µm) pasivo bajo [Ca++] control sin endotelio Cambio de presión hidrostática sin flujo Reflejo miogénico presión estiramiento del vaso receptores de estiramiento del músculo liso despolarización activación de canales de calcio voltajedependientes ICa liberación de Ca++ intracelular Músculo liso contracción muscular (-) Shear stress Respuesta del endotelio a cambios en el flujo. lumen vascular endotelio músculo liso Analisis del efecto del flujo sobre la vasculatura Efecto del caudal sobre el diámetro del vaso, a presión hidrostática constante. Kuo et al 1990 El caudal produce un aumento en el diámetro y este efecto depende del endotelio. Kuo et al 1990 Efecto del caudal y de la presión hidrostática sobre el diámetro (shear stress + miogénico). Kuo et al 1991 Efecto del caudal y de la presión hidrostática sobre el diámetro (shear stress + miogénico). El reflejo miogénico y el shear stress operan de manera antagónica regulado el diametro del vaso, y en consecuencia el caudal de sangre que pasa por dicha arteriola. Kuo et al 1991 El shear stress afecta la forma del endotelio pero no del músculo liso células endoteliales células de músculo liso El flujo causa un cambio en la forma de las células endoteliales producido por un rearreglo del citoesqueleto Nivel normalizado de mRNA de actina Malek et al 1994 Malek & Izumo 1996 Duración del shear stress (hs) Malek & Izumo 1996 Mediadores químicos del shear stress Las células endoteliales liberan prostaciclinas fosfolípidos fosfolipasa A2 ácido araquidónico vía de la ciclooxigenasa prostaciclinas Mediadores químicos del shear stress Las células endoteliales liberan óxido nítrico arginina oxido nítrico sintetasa óxido nítrico + citrulina + NADP El flujo evoca la generación de óxido nítrico en células endoteliales en cultivo. L-NNA, inhibidor de la óxido nítrico sintetasa Noris et al 1995 http://circres.ahajournals.org/content/76/4/536.full Efecto de dosis crecientes de L-NMMA (bloqueante de la síntesis de ON) sobre la conductancia vascular en ratas 0.3 mg/kg 1.0 mg/kg 3.0 mg/kg 10 mg/kg 30 mg/kg Gardiner et al 1990 Shear stress Un aumento en el flujo induce vasodilatación por liberación de NO shear stress lumen vascular Ca++ Ca++-calmodulina endotelio eNOS músculo liso NO ⇑cGMP relajación K+ Shear stress 2. Un aumento en el flujo induce vasodilatación por liberación de prostaciclina lumen vascular shear stress endotelio prostaciclina músculo liso ⇑cAMP relajación K+ Shear stress 1. Un aumento en el flujo induce vasodilatación por aumento en gK lumen vascular shear stress K+ endotelio hiperpolarización gK prostaciclina NO gap junctions relajación muscular músculo liso relajación EDHF: endotelial derived hyperpolarizing factor ET-1: endotelina PGI2: prostaciclina Shear stress Cuál es el sensor del flujo? lumen vascular endotelio músculo liso shear stress Endotelio vascular uniones oclusivas microtúbulos cadherinas integrinas lámina basal Reflejo miogénico ⇑ presión estiramiento del vaso despolarizacón del músculo liso Shear stress ⇑ flujo (-) ⇑ shear stress ⇑ gK, NO, prostaciclina ⇑gCa - ICa liberación de Ca++ intracelular contracción muscular (+) relajación del músculo liso vasodilatación El shear stress y el reflejo miogénico tienen efectos antagónicos que controlan el flujo vascular ⇑ shear stress ⇑P factores endoteliales miorelajantes reflejo miogénico importante en: cerebro riñón corazón 0 100 perfusion pressure (mm Hg) 200 CONTROL LOCAL DE LA RESISTENCIA DE LAS ARTERIOLAS BIOMECANICOS HUMORALES METABOLICOS • Reflejo miogénico • Shear stress • NO • Endotelina • Prostaciclina • O2, CO2 • Adenosina • Lactato •H+ • K+ • Temperatura Hiperemia activa: el aumento en la actividad metabólica de un tejido produce un aumento en el caudal sanguíneo que irriga a dicho tejido. Hiperemia activa Aumento en la irrigación sanguínea del músculo en función de la actividad física CONTROL LOCAL DE LA RESISTENCIA DE LOS CAPILARES Factores metabólicos FACTOR ORIGEN EFECTO O2 sangre vasoconstricción CO2 tejido vasodilatación K+ tejido (músculo) vasodilatación H+ tejido vasodilatación Adenosina tejido vasodilatación REGULACION METABOLICA DEL FLUJO SANGUINEO ⇑ metabolismo ⇓ [O2] tisular ⇑ [CO2] tisular (-) vasodilatación ⇓ resistencia ⇑ flujo de sangre hiperemia funcional o activa Regulación homeostática local + ⇑ tasa metabólica ⇓ pH ⇓ [O2] ⇑ liberación O2 a tejido vasodilatación humorales & biomecánicos hemoglobina ⇓ Afinidad O2 -Hb - + ⇓ resistencia ⇑ flujo de sangre ⇑ shear stress Intercambio gaseoso El pH afecta la interacción Hb-O2 Efecto Bohr Regulación homeostática ATP ⇑ actividad muscular + AMP ⇑ [adenosina]o adenosina vasodilatación receptores a Adenosina + ⇓ resistencia ⇑ flujo de sangre ⇑ shear stress INTERCAMBIO SANGRE - TEJIDOS INTERCAMBIO CON LOS TEJIDOS aorta arteriola capilar vénula vena v. cava REGULACION DEL FLUJO SISTEMICO DIFERENCIAL El intercambio se lleva a cabo a nivel de los capilares DIFUSION: pasaje de sustancias en el sentido que disipa el gradiente de concentracion. Ley de Fick F= DΔC DIFUSION FACILITADA: pasaje pasivo de sustancias en el sentido que disipa el gradiente de concentracion que requiere de un mecanismo de transporte. FILTRACION: movimiento de la solución en el sentido que disipa el gradiente de presión hidrostática. OSMOSIS: difusión pasiva del agua siguiendo su “grandiente” de concentración a través de una membrana semipermeable. TRANSPORTE ACTIVO: movimiento de solutos, normalmetne en contra del gradiente de concentración, a expensas de energía. TRANSPORTE TRANS-EPITELIAL transmembranal pericelular líquido intersticial plasma endotelio tejido capilar Endotelio vascular uniones oclusivas microtúbulos cadherinas integrinas lámina basal TRANSPORTE TRANS-EPITELIAL liposolubles hormonas esteroides O2 DIFUSION PASIVA CO2 líquido intersticial plasma endotelio tejido capilar TRANSPORTE TRANS-EPITELIAL DIFUSION FACILITADA hidrosolubles Na+ TRANSPORTE ACTIVO K+ glucosa TRANSPORTE VESICULAR H2O macromoléculas líquido intersticial plasma endotelio capilar tejido Transporte vesicular Transcitosis Transporte vesicular Transcitosis TRANSPORTE “VESICULAR” Qué se transporta? Cómo se discrimina? Macromoléculas Partículas Células Tamaño Carga Identidad - transcitosis mediada por receptor TRANSPORTE TRANS-EPITELIAL DIFUSION PASIVA (canales) DIFUSION FACILITADA hidrosolubles Na+ TRANSPORTE ACTIVO K+ glucosa TRANSPORTE VESICULAR macromoléculas FILTRACION líquido intersticial plasma endotelio tejido capilar ENDOTELIO VASCULAR uniones oclusivas microtúbulos cadherinas integrinas lámina basal CONEXIONES INTER-CELULARES Uniones oclusivas (tight junctions) capilar fenestrado capilar continuo capilar sinusoidal o discontinuo FILTRACION: FUERZA DE STARLING presión hidrostática presión oncótica π líquido intersticial plasma endotelio capilar Efecto de diferentes proteinas del plasma sobre la presión oncótica MW (kD) 70 140 400 tejido presión (mm Hg) FILTRACION: FUERZA DE STARLING filtración J = Kfc (Pc - Po)-σd (πc-πo)] coeficiente de filtración x coeficiente de reflexión FILTRACION: FUERZA DE STARLING Coeficiente de filtración: indica la conductancia hidráulica del endotelio. Coeficiente de reflexión: indica la dificultad con que un soluto atraviesa el espacio intercelular en comparación con el agua. Si σ = 1, la reflexión es total, el soluto no atraviesa. Si σ < 1, la reflexión es parcial, el soluto atraviesa parcialmente. El grado de porosidad de los capilares es diferente en diferentes tejidos: Cerebro: uniones estrechas, difusión restringida Hígado: gran porosidad que permite el paso de proteinas Intestino: intermedio Riñon: gran número de fenestrae que permiten el paso de solución acuosa a través de las células epiteliales. filtración & absorción x filtración (riñón) Barrera Hematoencefálica endotelio fenestrado endotelio continuo

